5.2.3.3 Intermetallische Phasen
Bisher haben wir im wesentlichen Teilchenkombinationen betrachtet, bei denen immer das Stammgitter einer Komponente aufgebaut worden ist. Nun tritt aber häufig der Fall auf, daß sich zwei Teilchenarten zusammentun, aber weder die Gitterstruktur der Ausgangskomponente noch die der zugegebenen Komponente bilden. Die gegenseitigen Kräfte wirken derartig, daß keines beider Gitter entsteht. Die zugegebene fremde Teilchenart ist zwar in der Lage, durch starke Kraftwirkungen das ursprüngliche Wirtsgitter zu verhindern, jedoch sind die Fremdatome kräftemäßig ebenso wenig in der Lage, ihr eigenes Gitter zu bilden. Folglich bauen beide Teilchensorten zusammen neue Gittertypen. Solche Substanzen mit neuartigen Gittern nennt man dann Intermetallische Phasen. Dabei können die Verteilungen der Teilchen wieder statistisch oder geordnet sein, die Schmelztemperaturen konstant oder nicht konstant sein.
Betrachten wir als Modellfall das Teilchenpaar Cu/Zn. Kupfer-Zink-Legierungen bis etwa 55 Atom% Zn werden als Messing bezeichnet.
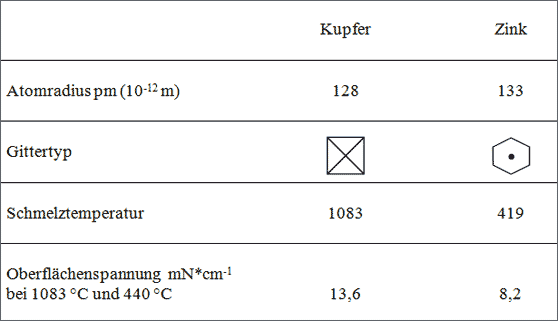
Tabelle 5.13: Einige Eigenschaften von Kupfer und Zink und der Atome
Die sehr wenig voneinander abweichenden Atomradien (vgl. Tab. 5.14) sprechen für eine gute Möglichkeit der Mischkristallbildung. Die Schmelztemperaturen und Oberflächenspannungen deuten auf starke Bindungen zwischen Cu-Atomen und auf schwache Bindungen zwischen Zn-Atomen hin. Aus dem Schmelzverhalten entspre-chender Legierungen läßt sich schließen, daß mittelstarke Kräfte zwischen Cu- und Zn-Atomen herrschen. Die Gitter der einzelnen Komponenten unterscheiden sich, eine lückenlose Mischkristallreihe ist nicht möglich.
Wir verfolgen nun ein kubisch flächenzentriertes Kupfergitter mit steigendem Angebot von Zn-Atomen bei ungefähr 300°C. Da die Teilchen nahezu gleich groß und die Kräfte zwischen beiden mittelstark sind, wird sich ein Kupfer-Substitutionsmischkristall bilden. Die Zn-Atome besetzen die Cu-Plätze zunächst anstandslos, denn die Kräfte der Zn-Atome untereinander sind so schwach, daß sie nicht in der Lage sind, gegen die Kräfte der Cu-Atome das eigene Zinkgitter zu bauen: Das ist nur bis zu 39 Atom% Zn möglich. Diese Mischkristalle werden mit dem Buchstaben α bezeichnet.
Betrachten wir das Abkühlen einer Schmelze mit 61 Atom% Cu und 39 Atom% Zn: Alle Teilchen setzen sich zu Kupfer-Mischkristallen mit einem kubisch flächenzen-trierten Gitter zusammen (vgl. (1) in Abb. 5.47). Geben wir aber mehr als 39 Atom% Zn in den Topf, dann sind die Cu-Atome bereits so stark von Zn-Atomen umgeben und kräftemäßig überfordert, daß sie nicht mehr alle Zn-Atome in den Mischkristall aufnehmen können. Einige Zn-Atome machen sich dann selbständig und bauen zusammen mit einigen Cu-Atomen ein neues Gitter, einen eigenen Kristall. Allerdings schaffen es die Zn-Atome nicht, die Bauweise der hexagonal dichtesten Kugelpackung durchzusetzen. Es gelingt ihnen lediglich das angestammte Cu-Gitter zu verzerren, zu stauchen. Das veranlaßt die Cu-Atome, sich gemeinsam mit den Zn-Atomen in der kubisch raumzentrierten Packung zusammenzusetzen (vgl. (2) in Abb. 5.47).
Dieser Kristall wird mit dem Buchstaben β bezeichnet. Bei niedrigen Temperaturen tritt sogar eine Überstruktur auf, so daß jedes Cu-Atom von 8 Zn-Atomen und jedes Zn-Atom von 8 Cu-Atomen umgeben ist (2). Das bedeutet ein Zahlenverhältnis 1:1, also 50 Atom% Cu und 50 Atom% Zn im Kristall.
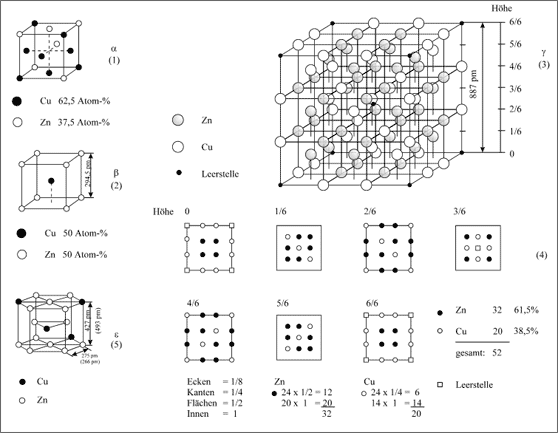
Abbildung 5.47: Mögliche Strukturen eines Cu/Zn-Systems (α,β,γ,ε-Messing)
![]()
Letzten Endes entsteht aufgrund der "Gitterstreitigkeiten" zwischen den beiden Teilchenarten die unterschiedliche Kristallstruktur. In diesem Zusammenhang nennt man solch einen Kristall allgemein eine Intermetallische Phase.
Genau genommen ist das kubisch raumzentrierte Gitter von 46-50 Atom% Zn be-ständig, der Homogenitätsbereich dieser Intermetallischen Phase beträgt 46-50 Atom% Zn. Zwischen 39 Atom% und 46 Atom% Zn besteht eine Mischungslücke. Dieses Spiel wiederholt sich im Prinzip noch dreimal mit fortschreitendem höheren Angebot an Zn-Atomen.
Bei einem mäßigen Überangebot von über 50 Atom% Zn hinaus bildet sich neben dieser einfachen kubisch raumzentrierten Kristallsorte ein weiterer, Zinkreicher Kristall mit einem komplizierten Gitter, das aber sehr an die kubisch raumzentrierte Form erinnert. Die Elementarzelle kann man sich durch Aneinandersetzen von je drei kubisch raumzentrierten Zellen in den drei senkrechten Raumachsen vorstellen (vgl. (3) in Abb. 5.47). Da jede von 27 üblichen raumzentrierten Elementarzellen zwei Teilchen enthält (8 *1/8 + 1 = 2), besteht die große Zelle aus 27 * 2 = 54 Teilchen. Zwei Plätze bleiben aber charakteristischer Weise unbesetzt - diese zwei leeren Gitterplätze oder Leersteellen (8 * 1/8 + 1 = 2) sind keine Fehler, sondern im Bausystem eingeplant (vgl. (4) in Abb. 5.47): die große Elementarzelle enthält also nur 52 Atome.
Dieser Messingkristall wird mit dem Buchstaben γ bezeichnet. Im Vergleich mit der einfachen kubisch raumzentrierten Anordnung ist dieser Kristall etwas stärker aufgeweitet. Die kleine kubische α-Zelle besitzt eine Kantenlänge von 294,5 pm, die Kantenlänge der großen Zelle ist allerdings nicht dreimal so lang, also 883,5 pm, sondern beträgt durchschnittlich 887 pm. Das läßt auf andere Bindekräfte und Bin-dungsverhältnisse schließen.
Den geregelten, nahezu harmonisch geordneten Aufbau dieser γ-Messing-Phase erkennt man erst, wenn man die gesamte Elementarzelle in Höhenabständen von 1/6 der Zellenhöhe in Scheiben schneidet (vgl. (4) in Abb. 5.47). Es ist nun besser zu erkennen, daß von den 52 Atomen 32 Zn-Atome sind (62,5 Atom% Zn) und 20 Cu-Atome (37,5 Atom% Cu). Der Homogenitätsbereich, in dem man das Cu/Zn-Verhältnis variieren kann, liegt zwischen 58 und 68 Atom% Zn.
Wiederum bei etwas höherem Angebot als 68 Atom% Zn erzwingen die Zn-Atome, die nicht in den γ-Kristall eingebaut werden können, eine neue Gitterkonstruktion. Diesmal setzen sie sich mit ihren Kräften soweit durch, daß tatsächlich eine hexagonale Form gebaut wird. Das geschieht im Konzentrationsbereich von 78 - 86 Atom% Zn. Es ist erstaunlich, welchen Kräfteeinfluß die wenigen Cu-Atome noch auf die Zn-Atome ausüben, sodaß die Zn-Atome ihre exakte hexagonal dichteste Packung nicht aufzubauen vermögen. Die hexagonale Zelle dieses Kristalls, der den Buchstaben ε bekommt, ist im Verhältnis zur echten dichtesten Packung gestaucht, sie ist zu breit und zu niedrig. Das zeigen die Gitterabmessungen im Kristall (vgl. (5) in Abb. 5.47).
Erst bei weiterem erhöhten Angebot von über 96 Atom% Zn hinaus bündeln die nicht am ε-Kristall beteiligten Zn-Atome alle ihre eigenen Bindekräfte und formieren ihr eigenes Gitter der hexagonal dichtesten Kugelpackung. Sie bauen bis 2 Atom% Cu mit in ihren Verband ein, so daß diese Kristalle als echte Zink-Mischkristalle anzusprechen sind. Für diesen Mischkristall liegt der Homogenitätsbereich zwischen 98 und 100 Atom% Zn. Die Abmessungen der hexagonalen Elementarzelle sind nun richtig. Die Zelle ist höher und schmaler als die Zelle des ε-Kristalls, wie bereits vorher angegeben. Diese Kristallsorte wird mit dem Buchstaben η bezeichnet.
Die Betrachtung des ε- und η-Kristalls ist deshalb besonders herauszuheben, weil hier demonstriert wird, welche Unterschiede zwischen Kupfer-Zink-Legierungen resultieren können. Obwohl die Teilchenarten gleich und die Anordnungen fast gleich sind, bewirken die verschiedenen Atomzahlen unterschiedliche Bindekräfte, andere Gitterabmessungen und deshalb naturgemäß auch andere Eigenschaften der Kristalle.
Die β-, γ- und ε-Kristalle werden als Intermetallische Phasen bezeichnet, da sie weder das Gitter des Kupfers noch das Gitter des Zinks besitzen. Als übersichtliche Darstellung der Möglichkeiten, Cu- und Zn-Atome zusammenzusetzen, bietet sich das Konzentrationsband an. Wir wählen die Kristallsorten, wie sie Experimente bei ca. 300 °C ergeben (vgl. Abb. 5.48). Hervorzuheben ist, daß am Rande links und rechts des Konzentrationsbandes immer die Mischkristalle auftreten, soweit sie existieren. Sie müssen ja kontinuierlich in die reinen Metallkristalle, die durch die senkrechten Begrenzungsstriche symbolisiert sind, überführt werden können. Die Intermetallischen Phasen sind dann durch Mischungslücken von den Mischkristallen getrennt. Das ist eine allgemeine Aussage, die für alle diese Konzentrationsbänder und später für Temperatur-Diagramme gilt.
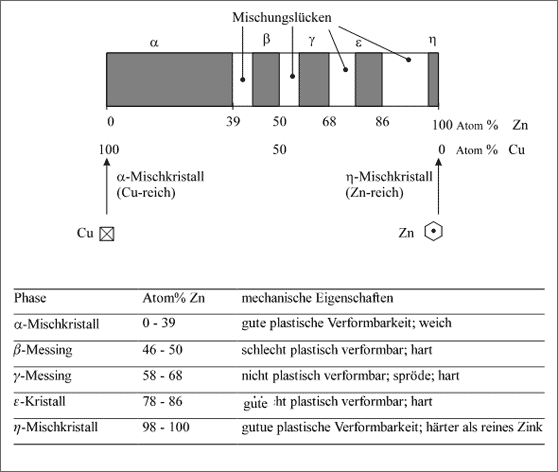
Abbildung 5.48: Mischkristallreihe und Intermetallische Phasen des Cu/Zn-Systems
Aus dem Konzentrationsband der Abbildung 5.48 läßt sich folgendes ablesen:
1. Konzentrationsbereiche links und rechts an beiden Rändern, die den Wirtsgittern der reinen Metalle und deshalb diesbezüglichen Mischkristallen entsprechen. Bei einem Teilchenangebot von 80 Atom% Cu und 20 Atom% Zn werden beim Abkühlen dieser Schmelze homogene α-Mischkristalle entstehen.
2. Konzentrationsbereiche, die in der Mitte liegen und homogene Kristalle anzeigen: es sind Intermetallische Phasen. Bei einem Teilchenangebot in einer Schmelze von 40 Atom% Cu und 60 Atom% Zn werden beim Abkühlen homogene γ-Mischkristalle entstehen.
3. Die Voraussage, welche Kristallsorten man erhält, wenn das Teilchenangebot keinem homogenen Kristall entspricht. Wählt man ein beliebiges Zahlenverhältnis, das eine Mischungslücke trifft, dann erhält man die beiden Kristallsorten, die der Mischungslücke benachbart sind. Bei einem Angebot von 40 Atom% Zn neben Kupfer werden hauptsächlich α-Kristalle entstehen und nur wenig β-Kristalle. Bei einem Wert nahe der β-Grenze, beispielsweise 45 Atom% Zn, werden überwiegend β-Kristalle entstehen und wenig α-Mischkristalle.
Das System Cu/Zn soll als Beispiel für eine große Anzahl weiterer ähnlicher Kombinationssysteme dienen, bei denen Intermetallische Phasen auftreten. Die Konzentrationsbänder anderer Metallpaare wie Cu/Sn (Bronze), Cu/Al, Mg/Al sind hauptsächlich in Büchern der Metallographie, der Werkstoffkunde und ausführlichen Lehrbüchern der Anorganischen Chemie zu finden.
![]()


