Vorwort
Materie ist diskontinuierlich aufgebaut - aus Atomen, Ionen oder Molekülen, die Strukturen der Teilchenverbände können infinit oder finit beschaffen sein. So sind etwa Kristalle von Metallen und Legierungen endlos dreidimensional aus Metall-Atomen aufgebaut (vgl. Band 2: Struktur der Metalle und Legierungen). In Salzkristallen sind die Teilchen ebenfalls infinit dreidimensional verknüpft, und zwar Ionen mindestens zweier Sorten zu einem Ionengitter (vgl. Band 4: Ionenkristalle mit einfachen Gitterbausteinen). Diese Teilchenverbände sind deshalb infinit aufgebaut, weil die zugrunde liegenden Metall-Atome und Ionen ungerichtete Bindefähigkeiten aufweisen: Sie umgeben sich mit so vielen Teilchen, wie geometrisch Platz vorhanden ist und ein Gleichgewicht der Bindekräfte erreicht wird. Die Koordinationszahlen lauten oftmals 6, 8 oder 12.
Nichtmetall-Atome sind durch das Vorhandensein gerichteter Bindekräfte gekennzeichnet. Sie ordnen sich sowohl in infiniten als auch in finiten Teilchenverbänden an. So lassen sich etwa die Verbände von C-Atomen in Diamant und Graphit als infinite Gitterstrukturen beschreiben, während die neu entdeckte dritte Kohlenstoff-Modifikation aus finiten Molekülen besteht: von den Fullerenen sind die C60-Moleküle am bekanntesten.
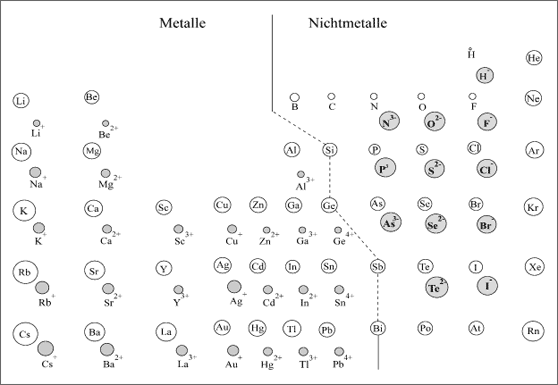
Abbildung aus Band 1: Atome und Ionen - Grundbausteine der Materie
Im Allgemeinen bilden die Nichtmetall-Atome kleine Moleküle nach bestimmten Verknüpfungsregeln: so stellt man sich etwa CH4-Moleküle, NH3- oder H2O-Moleküle aus den jeweiligen Atomen verknüpft vor. Das bereits im Band 1 abgebildete und hier erneut aufgenommene Periodensystem der Elemente zeigt eine Auswahl von Atomen und Ionen als Grundbausteine der Materie, die es nach bestimmten, in Band 1 ausführlich beschriebenen Verknüpfungsregeln gedanklich zu verknüpfen gilt.
Im Band 2 werden in der Vorstellung Metall-Atome “links und links im PSE” verknüpft, im Band 4 Ionen “links und rechts im PSE”. Im vorliegenden Band sollen die Nichtmetall-Atome auf der rechten Seite des Periodensystems zu Molekülen und Gittern verknüpft werden: “rechts und rechts im PSE”. Wie im Einführungsband bereits beschrieben, werden zur Verknüpfung die Normbindefähigkeiten zugrunde gelegt: das C-Atom besitzt maximal vier Bindefähigkeiten, das N-Atom meistens drei, das O-Atom zwei und das H-Atom nur eine Bindefähigkeit.
Die Lehrmittelfirmen haben auf der Grundlage dieser Anzahl von Bindefähigkeiten verschiedene Baukästen entwickelt. Meistens sind es “Kugel-Stab-” oder “Kugel-Druckknopf-Modelle”, die gut geeignet sind, räumlich gerichtete Bindungen zwischen mehreren Kugeln herzustellen und damit Molekülmodelle für einfach gebaute Moleküle zu veranschaulichen. Falls ein solcher Baukasten zur Hand genommen wird, ist das Verstehen des Textes für den Quereinsteiger sehr anschaulich !
Ein diesbezüglicher Hinweis: Anschaulichkeit und Quereinstieg sind deshalb möglich, weil das vorliegende Konzept der Normbindefähigkeiten ohne ein diffenziertes Atommodell, ohne die elektronentheoretische Interpretation der chemischen Bindung auskommt. Ein Bindestrich im Struktursymbol steht deshalb für das Modell einer Normbindefähigkeit, nicht für ein Elektronenpaar ! Selbstverständlich sind aus denselben Gründen Striche als Modelle für freie Elektronenpaare mit Absicht nicht vorhanden, sind im Rahmen des Modells der Normbindefähigkeiten sinnlos: der Quereinstieg in die Welt der Moleküle erfolgt ohne abstrakte und aufwendige Verabredungen zu Atombau und Chemischer Bindung !
![]()


