6.2.4 Atome der 5. Hauptgruppe
Die 5. Hauptgruppe besitzt keinen besonderen Namen, sie wird meistens nach der ersten Teilchensorte, dem Element Stickstoff benannt: Stickstoffgruppe. Es folgen Phosphor (P), Arsen (As), Antimon (Sb), Bismut (Bi). Alle genannten Atomsorten betätigen minimal drei gerichtete Normbindefähigkeiten, die alle drei zueinander gewinkelt sind: immer zwei Normbindefähigkeiten bilden zueinander den Winkel von ca.109,5° (vgl. (1) in Abb. 6.3). Man kann sich die Struktur dieser Atomsorten mit ihren Normbindefähigkeiten modellmäßig als eine Pyramide vorstellen, die ein gleichseitiges Dreieck als Grundfläche besitzt.
Bei dieser Hauptgruppe macht sich aber bereits bemerkbar, daß die Trennungslinie, die im Periodensystem die Metall-Atome von den Nichtmetall-Atomen abgrenzt, schräg durch das Periodensystem hindurch gezogen ist. Dadurch werden mehr oder weniger die Hauptgruppen getrennt, so daß der obere Teil der Hauptgruppe zu den Nichtmetallen, der untere zu den Metallen zählt. Dieser Effekt ist bei der 5. Hauptgruppe bereits dadurch ausgeprägt, daß das Bi-Atom auch relativ starke ungerichtete Bindekräfte wie ein Metall-Atom betätigen kann. Derjenige, der unbefangen ein Stück Bismut in die Hand nimmt, wird sofort erklären, es sei ein Stück Metall. Wir werden aber das Bismut als Nichtmetall beschreiben.
Drei Normbindefähigkeiten an einem Teilchen ermöglichen eine große Vielfalt von Teilchenkombinationen, von denen jedoch drei Konstruktionen eine besondere Rolle in der Praxis spielen. Deshalb wollen wir nur diese drei Grundkonstruktionen herausstellen: Hanteln, Tetraeder und netzartige Flächen.
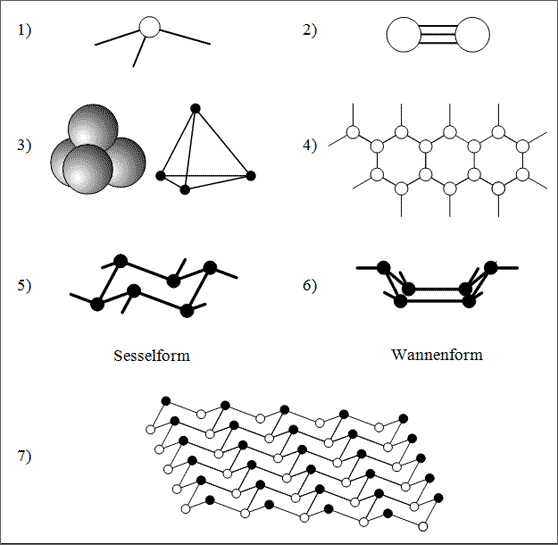
Abb.6.3: Modelle zur Verknüpfung von Atomen mit drei Bindefähigkeiten
Hanteln mit Dreifachbindung. Ebenso wie beim O-Atom Normbindefähigkeiten zu einer Bindekraft gebündelt und als Doppelbindung bezeichnet werden, so ist es bei einem Teilchen mit drei Normbindefähigkeiten auch möglich, die drei Normbindefähigkeiten zu einer Bindekraft zu koppeln und als Dreifachbindung zu bezeichnen (vgl. (2) in Abb. 6.3). Auch in diesem Falle handelt es sich um eine einzige Bindung von Atom zu Atom, die von drei Normbindefähigkeiten bewerkstelligt wird.
Tetraeder. Vier dicht gepackte Kugeln lassen sich mit Hilfe eines Tetraeders beschreiben, wie er auch in dichtesten Kugelpackungen vorkommt (vgl. Band 2): Jede Kugel berührt bei dieser Konstruktion drei andere Nachbarkugeln (vgl. (3) in Abb. 6.3). Im Gegensatz zu Tetraedern in Kugelpackungen existieren allerdings keine starken Bindekräfte mehr nach außen, denn diese sind bei gerichteten Bindungen abgesättigt. Auf trotzdem vorhandene ungerichtete Restbindekräfte kommen wir später noch zurück. Es ist besonders zu beachten, daß der Bindungswinkel zwischen den Atomen sehr klein ist, nämlich nur 60°. Das bezeichnen wir als ganz erhebliche “Verspannung” der Bindungen, wenn man als Durchschnittswinkel wiederum 109,5° annimmt. Die Bindungen sind deshalb nicht sehr stabil, sie “springen” in der Praxis relativ leicht auf. Aus diesem Grund ist in den meisten Molekülbaukästen dieser Bindungswinkel auch nicht vorgesehen.
Netzartige Flächen. Versucht man eine Bauweise zu Ketten wie bei Atomen der 6. Hauptgruppe, dann bleibt an jedem Atom eine gerichtete Bindefähigkeit frei. Durch Nebeneinanderreihen solcher Ketten erhält man flächenhafte Teilchenanordnungen, die aus Sechserringen zusammengesetzt erscheinen (vgl. (4) in Abb. 6.3). Im ersten Moment denkt man an ebene Sechserringe, die wiederum “verspannt” sein müßten, wenn man den Durchschnittswinkel 109,5° zugrunde legt. Deshalb werden solche ebenen Anordnungen von Atomen nicht realisiert.
Bei gewinkelten und deshalb “unverspannten” Sechserringen unterscheidet man allerdings zwei Möglichkeiten: Sesselform und Wannenform. Die abwechselnde Folge der beteiligten Kugeln “oben/unten/oben/unten/oben/unten” oder auch “up/down/up/down/up/down” ergibt einen sehr regelmäßig gebauten Ring, er wird als Sesselform bezeichnet (vgl. (5) in Abb. 6.3). Kippt man gedanklich den Ring nämlich leicht, so daß vier Kugeln in einer Ebene liegen, kann man sich mit viel Phantasie einen “Opasessel” mit Kopflehne und Fußstütze vorstellen.
Die nicht regelmäßige Abfolge “oben/unten/unten/oben/unten/unten” ist gleichbedeutend mit der Abfolge “unten/unten/oben/unten/unten/oben”: diese Form bezeichnet man als Wannenform (vgl. (6) in Abb. 6.3). Liegen gedanklich wiederum vier Kugeln in einer Ebene, kann man sich mit viel Phantasie eine Badewanne vorstellen. Diese Wannenform ist nicht geeignet, eine gleichmäßig aufgebaute netzartige Fläche zu bauen - das ist nur mit Sechsringen der Sesselform möglich (vgl. (4) oder (7) in Abb. 6.3).
Bei den Molekülstrukturen der Elemente der 5. Hauptgruppe, deren Atome jeweils drei gerichtete Normbindefähigkeiten betätigen, herrschen die drei Konstruktionstypen (2) bis (4) vor, nicht jede Konstruktion wird von jeder Atomsorte in gleicher Weise bevorzugt. Verfolgen wir die Teilchen der Hauptgruppe von oben nach unten, so ergeben sich folgende Regeln:
Die Tendenz zur Bildung von Hanteln nimmt von oben nach unten ab.
Die Tendenz zur Bildung von Tetraedern herrscht in der Mitte vor.
Die Tendenz zur Bildung von Sechseck-Flächen nimmt nach unten zu.
Stickstoff. N-Atome für sich allein bilden nur Hanteln mit Dreifachbindung, größere Verbände von N-Atomen mit Einfachbindungen oder Doppelbindungen sind unbekannt.
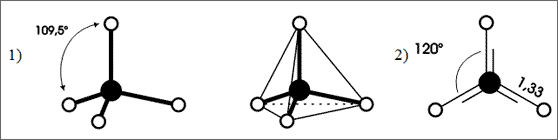
Abb. 6.4: Modelle zur Verknüpfung von Atomen mit 4 Bindefähigkeiten
Phosphor. P2-Hanteln sind zwar bekannt, aber sie bilden sich in der Praxis nur in unbedeutendem Maße. Dagegen kommen P4-Tetraeder vor: sie bauen weißen Phosphors auf. Flächige Konstruktionen, an denen Sechseckringe beteiligt sind, bilden sich ebenso leicht: Verknüpft man Sesselformen zu großen Flächen, so hat man die Struktur des schwarzen Phosphors vor Augen. Wannenform, Sesselform und Fünferringe in kunstvollem Zusammenbau führen zum violetten Phosphor. Alle möglichen Ringvarianten, zusammen mit verzerrten Tetraedern, Ketten und vielem anderen mehr, fast eine Tohowabohu-Konstruktion, bildet die Grundlage für den roten Phosphor.
Der Spezialist kennt noch mehr Varianten, die aber alle in ihrer Bauweise auf die genannten Grundmuster zurückzuführen sind. Diese Vielfalt beruht mit auf der besonderen Eigenschaft der P-Atome, die Bindungswinkel stark zu verändern bzw. “verspannen” zu können.
Liegen von gleichen Teilchensorten unterschiedliche Strukturen vor, so werden diese Strukturvarianten als Modifikationen bezeichnet. Die vier genannten Modifikationen, nämlich weißer, roter, violetter und schwarzer Phosphor, besitzen aufgrund ihrer verschieden Strukturen sehr unterschiedliche Eigenschaften: insbesondere der weiße Phosphor ist sehr giftig und entzündet sich an der Luft von selbst.
Arsen. As-Atome weichen der Bildung von Hanteln möglichst aus, sie verknüpfen sich eher zu Tetraedern und sind das Bauelement des gelben Arsens. Flächenelemente mit Sesselstruktur führen zum üblichen grauen Arsen.
Antimon. Hanteln und Tetraeder der Sb-Atome sind zwar bekannt, feste Substanzen dazu aber nicht. Die Grundstruktur des grauen Antimons läßt sich zurückführen auf die Anordnung der Sb-Atome in Flächen mit Sesselbauweise. Das Antimon wirkt bereits sehr metallisch.
Bismut. Strukturen mit Hanteln und Tetraedern sind nicht bekannt. Das ebenfalls wie das Antimon sehr metallisch wirkende Bismut ordnet die Bi-Atome in der Form von Flächen mit Sesselbauweise. Die Struktur entspricht der des grauen Antimons, des grauen Arsens und des schwarzen Phosphors.
![]()


