5.2.4.1 Edelstähle
Alle Stähle sind dadurch gekennzeichnet, daß die Fe-Atome teilweise blockiert und verspannt sind, oder daß komplette harte Kristalle mit in das Gefüge eingebaut sind. Eine besondere Rolle spielt dabei das "Umklappen" des kubisch flächenzentrierten Gitters des γ-Eisens in das kubisch raumzentrierte Gitter des α-Eisens. Enthält das γ-Eisen eingelagerte C-Atome, liegt also Austenit vor, dann entsteht durch schnelles Umklappen Martensit, ein sehr hartes und sprödes Material.
In vielen Fällen der Praxis werden allerdings die Eigenschaften des Austenits gewünscht, der aber bei Raumtemperatur nicht beständig ist - mit ca. 700 °C und 4 Atom% Kohlenstoff besitzt der Austenit seine niedrigste Umklapptemperatur. Ein Ausweg ist der Einbau anderer Atomsorten.
Wie bereits erörtert, bilden Eisen und Nickel Substitutionsmischkristalle, wobei Nickel selbst das kubisch flächenzentrierte Gitter besitzt. Je mehr Ni-Atome in das Eisengitter eingebaut werden, desto weniger kommen bei niedrigen Temperaturen die Kräfte der Fe-Atome zum Tragen, die das Gitter in das α-Eisen umzuklappen vermögen. Bei dieser Umwandlung eines Gitters der Koordinationszahl 12 in eines der Koordinationszahl 8 müssen Bindungen zwischen den Teilchen gelöst und wieder neu gebildet werden. Dies sei in (1) der Abb. 5.59 für die Quadratmaschenschichten symbolisch angedeutet (siehe auch Abb. 5.20).
Da nun die Bindekräfte zwischen Fe- und Ni-Atomen sehr stark sind, ist ihre Trennung allein durch die Kräfte der Fe-Atome nicht mehr möglich. Insofern kann durch entsprechende Substitution von Ni-Atomen auch der Austenit mit seinen eingelagerten C-Atomen am Umklappen gehindert werden (vgl. (2) in Abb. 5.59). Dadurch ist dann der substituierte Austenit kubisch flächenzentrierter Struktur auch bei niedriger Temperatur beständig und als Stahl zu verwenden. All diese Materialien werden austenitisch genannt. Zu ihnen zählen Edelstähle mit der Bezeichnung V2A, sie sind als Stähle für hochwertige Messerklingen und Kochtöpfe bekannt.
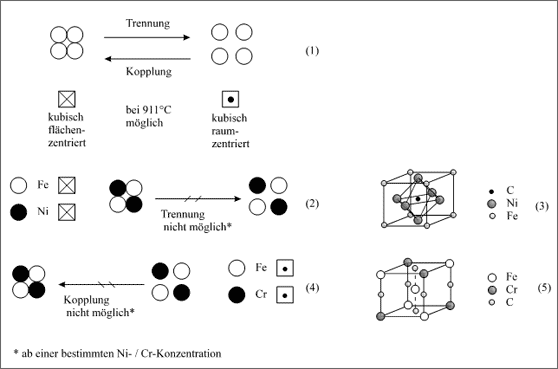
Abbildung 5.59: Modellvorstellungen für das Umordnen von Atomen zwischen α-Eisen und γ- Eisen und entsprechenden Ni- und Cr-Legierungen
Die Gitterkonstruktion können wir uns schematisch vorstellen (vgl. (3) in Abb. 5.59): Sie stellt den Überstrukturkristall dar, der aber nur mit einem relativ kleinen Homogenitätsbereich der Konzentration um 75 Atom% Nickel beständig ist. Die Elementarzelle zeigt entsprechend, daß von vier Metall-Atomen 6/2 Ni-Atome und nur 8/8 Fe-Atome vorhanden sind. In anderen Konzentrationsbereichen ist die Teilchenverteilung statistisch.
Den gegenteiligen Effekt der Ni-Atome erreicht man durch Substitution eines Teils der Fe-Atome durch Cr-Atome (vgl. (4) in Abb. 5.59) . Chrom selbst existiert ausschließlich als kubisch raumzentriertes Gitter und ist so mit dem α-Eisen gittermäßig identisch. Die Cr-Atome müssen besondere Kräfte besitzen, die den Bau des weniger dichten kubisch raumzentrierten Gitters begünstigen, ähnlich den Kräften der Fe-Atome. Der Ersatz von etwa 25 Atom% Eisen durch Cr-Atome bewirkt daher, daß das α-Eisen auch bei höheren Temperaturen nicht mehr in die γ-Struktur umklappen kann. Die schematische Gitterkonstruktion zeigt (5) in Abb. 5.59: Von den zwei Metall-Atomen der Elementarzelle sind 4/8 Cr-Atome und 3/2 Fe-Atome, also 25 Atom% Chrom.
![]()


