5.1.11 Chemische Symbole für Metallkristalle
Wenn wir häufig mit Metallen arbeiten und deren Eigenschaftsänderungen und Umwandlungen anhand der Atome deuten wollen, müssen wir oftmals über die Struktur informieren. Die beste Information ist das aus Kugeln gebaute Raummodell, es ist jedoch für jede einzelne Struktur zu aufwendig und unhandlich. Daher hilft man sich gern mit räumlichen Zeichnungen.
Um nur bezüglich der drei Metallstrukturen zu informieren, genügen die bereits aus Tabelle 3 bekannten Symbole:
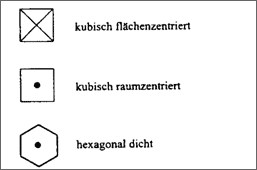
Wer jedoch diese Strukturen nicht kennt, kann aus den genannten Symbolen kaum Rückschlüsse ziehen. Deshalb haben die Kristallchemiker versucht, Symbole zu entwerfen, aus denen man die wichtigsten Strukturmerkmale erkennt. Sie sind einfach anzuwenden, schnell zu schreiben und lassen sich gut einprägen. Wichtigstes Strukturmerkmal ist die Zuordnung und Anzahl von direkten NachbarTeilchen, also die Koordinationszahl mit Koordinationspolyeder. Die Symbole da-für zeigt Tabelle 5.6 .
Außerdem können wir mit einem Symbol darstellen, daß es sich etwa bei einem Magnesiumkristall um ein dreidimensionales, unendliches Gitter handelt, in dem die Atome hexagonal mit der Koordinationszahl12 angeordnet sind:
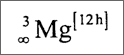
Die Symbole für die unendliche, dreidimensionale Bauweise werden vorangestellt, der Koordinationspolyeder wird oben rechts in eckigen Klammem angegeben. Da es sich bei den Metallen immer um eine unendliche, dreidimensionale Raumstruktur handelt, werden die entsprechenden Symbole meistens weggelassen. Wenn wir jemandem etwas über das Magnesium mitteilen, der die Struktur bereits genau kennt, können wir uns die Angabe des Koordinationspolyeders ebenfalls sparen. Es bleibt als magere Schrumpfinformation nur noch das Symbol Mg übrig. Wir wissen jetzt aber, welche Menge an Hintergrundinformation das Symbol Mg besitzt!
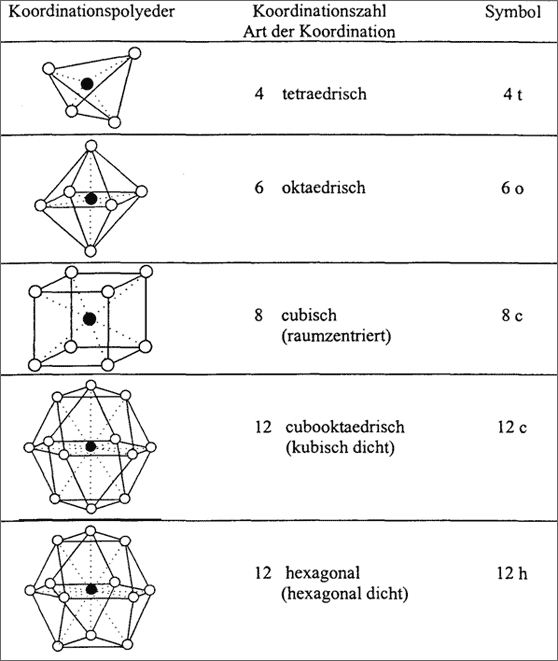
Tabelle 5.6: Symbole zur Information über wichtige StrukturmerkmaIe.
Was sagt uns das Symbol Fe? Es sagt uns nicht, ob Eisen-Atome kubisch flächenzentriert oder kubisch raumzentriert zusammengesetzt sind. Das können wir nun durch diese Symbole genauer mitteilen:
Fe[12c] oder Fe[8c] .
Wenn wir umgekehrt die folgenden Symbole lesen, sind wir besser informiert als durch Symbole wie Ag, Ti, Na oder Sn:
AG[12c], Ti[12h], Na[8c], Sn[4t]
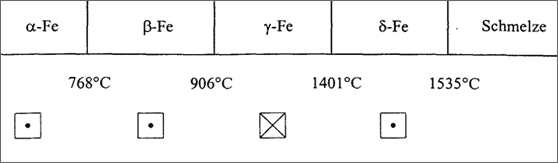
Abbildung 5.27: Verschiedene Eisenstrukturen in Abhängigkeit von der Temperatur
Ein ähnliches Informationssystem beruht darauf, die gegenseitigen Koordinationszahlen zweier benachbarter Teilchen rechts unten an das Teilchensymbol zu schreiben, beispielsweise:
[Fe8/8]∞
Diese Symbolik soll über ein unendliches Gitter von Eisen-Atomen informieren, bei dem ein Teilchen acht umgebende Nachbarn besitzt, diese Nachbarn aber ebenfalls wieder Diese Symbolik soll über ein unendliches Gitter von Eisen-Atomen informieren, bei dem ein Teilchen acht umgebende Nachbarn besitzt, diese Nachbarn aber ebenfalls wieder Diese Symbolik soll über ein unendliches Gitter von Eisen-Atomen informieren, bei dem ein Teilchen acht umgebende Nachbarn besitzt, diese Nachbarn aber ebenfalls wieder von acht Teilchen berührt werden: auch so kann über die kubisch raumzentrierte Eisenstruktur informiert werden. Das flächenzentrierte Gitter wird in diesem System dann folgendermaßen symbolisiert:
[Fe12/12]∞
Kristallisieren Metall-Atome einer Sorte in mehreren verschiedenen Gitteranordnungen, dann ist die Bauweise des Gitters vom Wärmeinhalt und damit vom Temperaturniveau abhängig. Wir haben das am Beispiel rur die Umwandlung des Eisens bereits erwähnt. Gitteranordnungen, die in bestimmten Temperaturbereichen spezielle Eigenschaften haben, werden numeriert, und zwar mit griechischen Buchstaben von der niederen zur höheren Temperatur (vgl. Abb. 5.27). a-Eisen existiert bis 768 oe, es besitzt ein kubisch raumzentriertes Gitter. Bis 906°e ändert sich zwar der Gitteraufbau nicht, das Eisen ist aber nicht magnetisch und wird als ß-Eisen bezeichnet. Ab 906°e ist das kubisch flächenzentrierte Gitter stabil und ab 1401°e bis zum Schmelzen wieder die kubisch raumzentrierte Anordnung.
Der griechische Buchstabe ist demnach keine Information über die Art eines bestimmten Gitteraufbaues an sich, sondern nur eine Numerierung: a- und ß-Eisen besitzen die gleiche Struktur. Welche Informationsart wir verwenden ist gleichgültig, sie muß nur dem jeweiligen Informationszweck angepaßt sein. So können wir rur die Substanz Eisen mit dem kubisch raumzentrierten Gitter wahlweise die Informationen
Fe[8c] oder [Fe8/8]∞ oder α-Fe
verwenden. Es steht aber offen, durch beliebige verständliche Zusätze die Information zu erweitern und zu verbessern.
![]()


